Kuis 6. Kerjakan 1 problem (per chapter) dari tugas kelompok lain (Chapter 13 s/d 18).
Chapter 13
Diketahui persamaan reaksi A + 3B → 2C + 2D Molaritas B mula-mula 0,9986 M dan dalam waktu 13,2 menit molaritas B berubah menjadi 0,9746 M. Berapa kecepatan reaksi rata-rata selama waktu tersebut dalam M per detik.
Pembahasan :
Molaritas B berubah selama reaksi berlangsung 13,2 menit dapat dihitung sebagai berikut.
Δ[B] = 0,9746 M – 0,9986 M
= –0,0240 M
Δt = 13,2 menit

Chapter 14
Persamaan laju dari reaksi aA → bB dapat dituliskan
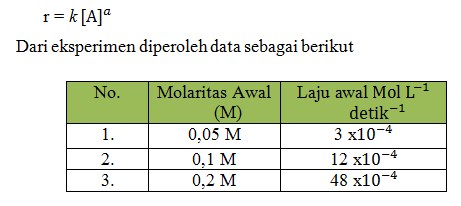
Tentukan orde reaksi!
Pembahasan :
Jika reaksi tersebut memiliki orde reaksi terhadap a = 1, maka laju reaksi sebanding dengan molaritas [A] , yaitu r = k[A]
Hal ini tidak mungkin, karena pada molaritas awal nomor 2 ketika molaritas awal dinaikan 2 kali, laju awal 4 kali lebih besar. Orde reaksi dapat dicari dengan cara membandingkan laju reaksi dari masing-masing.

Chapter 15
Hitunglah kelarutan molar PbI2 dalam larutan KI 0,1 M. (Ksp PbI2 = 7,1 × 10−9)
Pembahasan :
Dalam larutan, KI akan terdisosiasi menjadi ion K+ dan ion I−. Pada larutan KI 0,1 M, [I−] = 0,1 M. Asumsikan s adalah jumlah mol PbI2 yang larut menghasilkan 1 L larutan jenuh, sehingga terdapat tambahan s mol Pb2+/L dan 2s mol I−/L
PbI2(s) ⇌ Pb2+(aq) + 2I−(aq)

Oleh karena dapat diduga bahwa s ≪ 0,1, maka dapat diasumsikan (0,1 + 2s) ≈ 0,1
 Jadi, kelarutan molar PbI2 dalam larutan KI 0,1 M adalah 7,1 × 10−7 mol/L
Jadi, kelarutan molar PbI2 dalam larutan KI 0,1 M adalah 7,1 × 10−7 mol/L
Chapter 16
Jika kelarutan Ca(OH)2 dalam air adalah s mol L-1, maka hasil kali kelarutan Ca(OH)2..
Pembahasan :
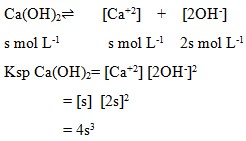
Chapter 17
Jika konsentrasi Ca+2 dalam larutan jenuh CaF2 = 2 x 10-4 mol L-1, maka hasil kali kelarutan CaF2..
Pembahasan :
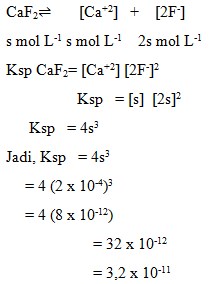
Chapter 18
Pada suhu tertentu 0,350 g BaF2 (Mr = 175) melarut dalam air murni membentuk 1 liter larutan jenuh. Hasil kali kelarutan BaF2 pada suhu itu adalah…
Pembahasan :
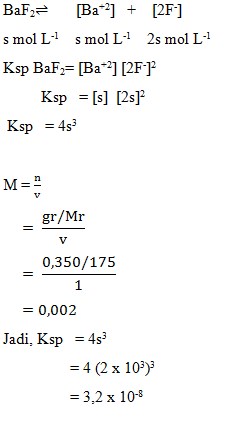


Tidak ada komentar:
Posting Komentar