Latihan 6. Kerjakan 1 example (per chapter) dari tugas kelompok lain (Chapter 13 s/d 18).
Chapter 13
Kenapa Kenaikan suhu akan mempercepat laju reaksi?
Pembahasan :
karena Kenaikan suhu akan mempercepat laju reaksi dikarenakan energi kinetik partikel-partikel yang bereaksi semakin tinggi. Apabila suhunya menurun maka energi kinetik partikel-partikel yang bereaksi semakin kecil.
Chapter 14
Katalis alami apa yang sering digunakan dalam pembuatan asam sulfat?
Pembahasan :
V2O5 merupakan katalis alami yang digunakan untuk sintesis asam sulfat.
Pt juga merupakan katalis pembuatan asam sulfat tetapi perlu diproses kembali terlebih dahulu.
Chapter 15
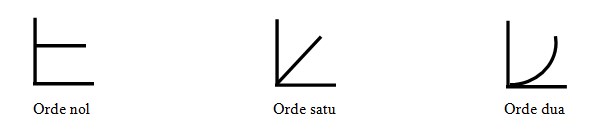
Gambarkan grafik yang menyatakan reaksi orde nol,satu dan dua!
Pembahasan :
Chapter 16
Suatu katalis mempercepat reaksi dengan cara meningkatkan?
Pembahasan :
jumlah molekul yang memiliki energi di atas energi aktivasi karena jumlah molekul yang memiliki energi di atas energi aktivasi dan menurunkan energi aktivasi sehingga reaksi dapat terjadi lebih cepat.
Chapter 17
Energi aktivasi suatu reaksi dapat diperkecil dengan cara?
Pembahasan :
- Luas permukaan, semakin luas permukaan semakin cepat reaksi terjadi.
- Suhu, semakin tinggi suhu semakin cepat reaksi terjadi karena energi kinetiknya bertambah melebihi energi aktivasi .
- Konsentrasi, semakin besar konsentrasi, semakin cepat terjadi reaksi karena semakin banyak molekul-molekul bertumbukan (berinteraksi)
- Katalis, berfungsi mempercepat terjadinya reaksi karena katalis dapat menurunkan energi aktivasi.
Chapter 18
Suatu reaksi berlangsung dua kali lebih cepat setiap suhunya dinaikkan 10°C. Jika laju reaksi pada saat suhu 20°C adalah x M/detik, tentukan laju reaksi pada saat suhu dinaikkan menjadi 60°C.
Pembahasan :
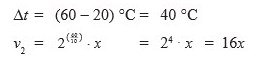


Tidak ada komentar:
Posting Komentar